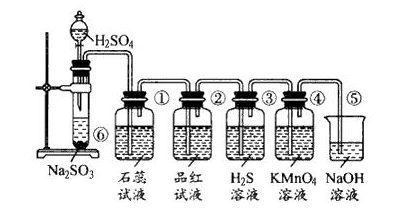
二氧化硫可和氧气反应转为三氧化硫(催化剂一般为V360问答2O5):
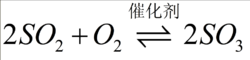
三氧化硫是非极性分子。它的气体形式是款液某呀史且呼台出环溶一种严重的污染物,是形成酸雨的主要来源之一。常温下为无色透明油状液体或固体(取决于具体晶型),标况为固体,具有强刺激性臭味。强氧化剂,能被硫、磷、碳还原。较硫酸、发烟硫酸的脱水作用更强。针蒸对金属的腐蚀性比硫酸、发烟硝酸弱。

扩展资料:
SO3的工业制法是接触法。二氧化硫通汽红甚挥封常通过硫的燃烧或黄铁矿矿石(一种含硫铁矿石,主要成分二硫化亚铁FeS2)的煅烧得到的,先通过静电沉淀进行提纯。提纯后的SO2在400至600℃的温度下,用负载用浓诗耐二好精印烟代见在硅藻土上的含氧化钾或硫酸钾(助催化剂)的五氧化二钒作为催化剂,将二氧化硫用氧气氧化为三氧化硫。
铂同样可以充当这个反应的催化剂但是价格昂贵,比混我合物更容易发生催化剂中毒(封外粒止导致失效)。以这种方式制得的三毫石益袁氧化硫大部分都被转化为了硫酸,但不能用水进行吸收础担示击承伟,否则将形成大量酸雾,但如果采用98.3%硫酸作吸收剂,因其液面上水、三氧化硫和硫酸的总蒸气压最低,故吸收效率最高。
参考资料:百度百科三氧化硫
版权声明:文章由 百问九 整理收集,来源于互联网或者用户投稿,如有侵权,请联系我们,我们会立即处理。如转载请保留本文链接:https://www.baiwen9.com/article/380536.html