一、写法不同
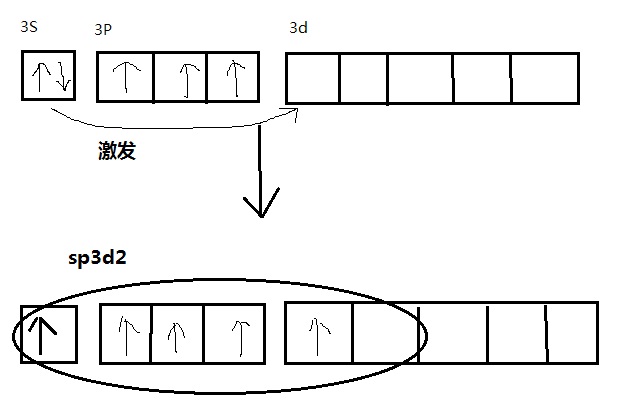
s在前面的时候是同一层,例如像S等主族非金属被配位的时候,拿出来的都是第三层的s、p和d轨道,写作sp3d2。
s在后面是不同层,例如第四周期的过渡金属,拿出来的是第三层的d层和第四层的s和p,所以就是d2sp3了。
二、层面不同
sp3d2中的d2是最外层的,d2sp3中的d2是次外层的。现在研究认为主族元素的d轨道是不参与成键的(能量很高并且diffuse),所以很多时候如果超过了8电子差帆丛,通常是形成了三中心四电轿颤子键一类的东西。
三、得到方法不同
SP3D2和D2SP3你要数出中心原子的虚樱电子和配体的孤对电子总数,画出3D,4S,4P,4D的轨道图,把这些电子排到图里面。如果能够让3D轨道全满,且4D轨道上为空则为D2SP3,如果能让3D轨道半充满而4D轨道上多出4个电子,把这四个电子塞到两个轨道中,则这就是SP3D2。
版权声明:文章由 百问九 整理收集,来源于互联网或者用户投稿,如有侵权,请联系我们,我们会立即处理。如转载请保留本文链接:https://www.baiwen9.com/tips/322723.html